Comment les cellules s’adaptent-elles à une carence en sucre ?
L’équipe de Sébastien Léon à l’Institut Jacques Monod (UMR université Paris Diderot, CNRS) dévoile un nouveau mécanisme qui contrôle, chez la levure, la dégradation des transporteurs de sucre localisés à la surface des cellules. Ce mécanisme fait intervenir Csr2, une protéine de la famille des arrestines qui est régulée à plusieurs niveaux par la disponibilité en glucose. Ce travail, réalisé en collaboration avec le laboratoire de Libuše Váchová et Zdena Palková à l'Université Charles à Prague, a été publié le 3 mai 2017 dans la revue Journal of Cell Biology.
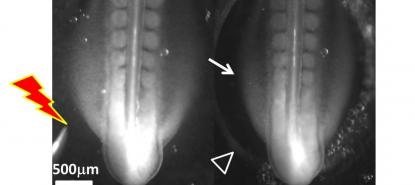
Les cellules sont délimitées par une membrane, appelée membrane plasmique, dans laquelle sont insérées des protéines transporteurs qui permettent aux différents nutriments de pénétrer à l’intérieur de la cellule. En fonction de l’évolution des conditions nutritionnelles de l’environnement, certains de ces transporteurs deviennent inutiles. Ils sont donc dégradés par la cellule grâce à un mécanisme appelé endocytose.
Le mécanisme d’endocytose est très bien caractérisé chez la levure de boulanger Saccharomyces cerevisiae. Comme les cellules humaines, la levure possède à sa surface des transporteurs dont elle doit réguler l’abondance en utilisant les mêmes mécanismes que les cellules humaines. La levure utilise un sucre, le glucose, pour produire l’énergie nécessaire à sa croissance.
Les chercheurs ont caractérisé un nouveau mécanisme qui permet la dégradation des transporteurs de glucose lorsque les levures sont soumises à une carence dans ce sucre. Ce mécanisme dépend de Csr2, une protéine de la famille des arrestines. Chez l’Homme, les arrestines sont d’importants régulateurs du métabolisme et certaines d’entre elles sont des suppresseurs de tumeur, c’est à dire que leur absence peut causer des cancers. Il est donc très important de comprendre le rôle de ces arrestines et leur régulation par la physiologie cellulaire.
Les chercheurs ont découvert que Csr2 est fabriquée et devient active uniquement en absence de glucose. Son activité est régulée par de nombreuses modifications post-traductionnelles. Cette régulation complexe fait intervenir plusieurs acteurs (voies de signalisation PKA, AMPK) dont l’activité est elle même régulée par la disponibilité en glucose. Ainsi, cette étude montre que la régulation d’une arrestine par la signalisation cellulaire contribue à l’homéostasie des transporteurs et donc à l’adaptation des cellules à leur environnement.
Publication
Multilevel regulation of an α-arrestin by glucose depletion controls hexose transporter endocytosis
Hovsepian J, Defenouillère Q, Albanèse V, Váchová L, Garcia C, Palková Z, Léon S.
J Cell Biol. 2017 May 3
Source : INSB CNRS