Une enzyme pas comme les autres
Chez les plantes comme chez les animaux, l’ADN est associé à des protéines histones qui permettent de compacter l’ADN à l’intérieur des cellules. Ces protéines histones portent différentes modifications chimiques dont le rôle va être soit de réprimer l’expression des gènes, soit de réprimer les éléments génétiques mobiles c’est-à-dire les séquences d'ADN capables de se déplacer de manière autonome dans un génome.
Des chercheurs de l’Institut Jacques Monod (Université de Paris, CNRS) se sont intéressés au fonctionnement des protéines qui mettent en place les modifications chimiques sur les histones chez la paramécie, un eucaryote unicellulaire. Ils ont ainsi caractérisé les propriétés inédites d’une enzyme qui catalyse non pas une mais deux modifications silencieuses différentes. Ces travaux, publiés dans la revue Nature Communications, révèlent que ces deux modifications partagent un rôle ancestral commun qui réduit au silence les éléments génétiques mobiles (également appelés éléments transposables).
Dans nos cellules, le génome est compacté et organisé dans le noyau grâce aux protéines histones. Ce complexe ADN-protéines, appelé chromatine, est important dans le déroulement de nombreux processus cellulaires, en particulier le contrôle de l’expression des gènes. En effet, les histones peuvent porter des modifications chimiques, qui sont associées à des états héritables de l’expression des gènes.
« Par exemple, l’histone H3 est porteuse de deux modifications. La première (la triméthylation de la lysine 27- H3K27) maintient réprimée l’expression de gènes durant le développement et joue un rôle crucial dans le contrôle épigénétique du développement. La deuxième (la triméthylation de la lysine 9 - H3K9) est quant à elle, associée à des régions génomiques silencieuses différentes, qui comportent, non pas des gènes, mais des séquences répétées de l’ADN, telles que des éléments transposables. » explique Sandra Duharcourt, directrice de recherche à l’Institut Jacques Monod. Chez les plantes et les animaux, ces deux modifications silencieuses sont en général mises en place par des enzymes différentes.
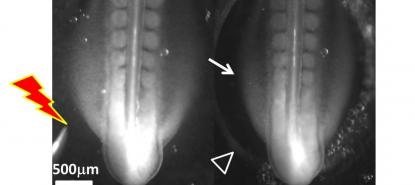
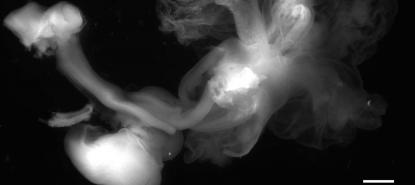
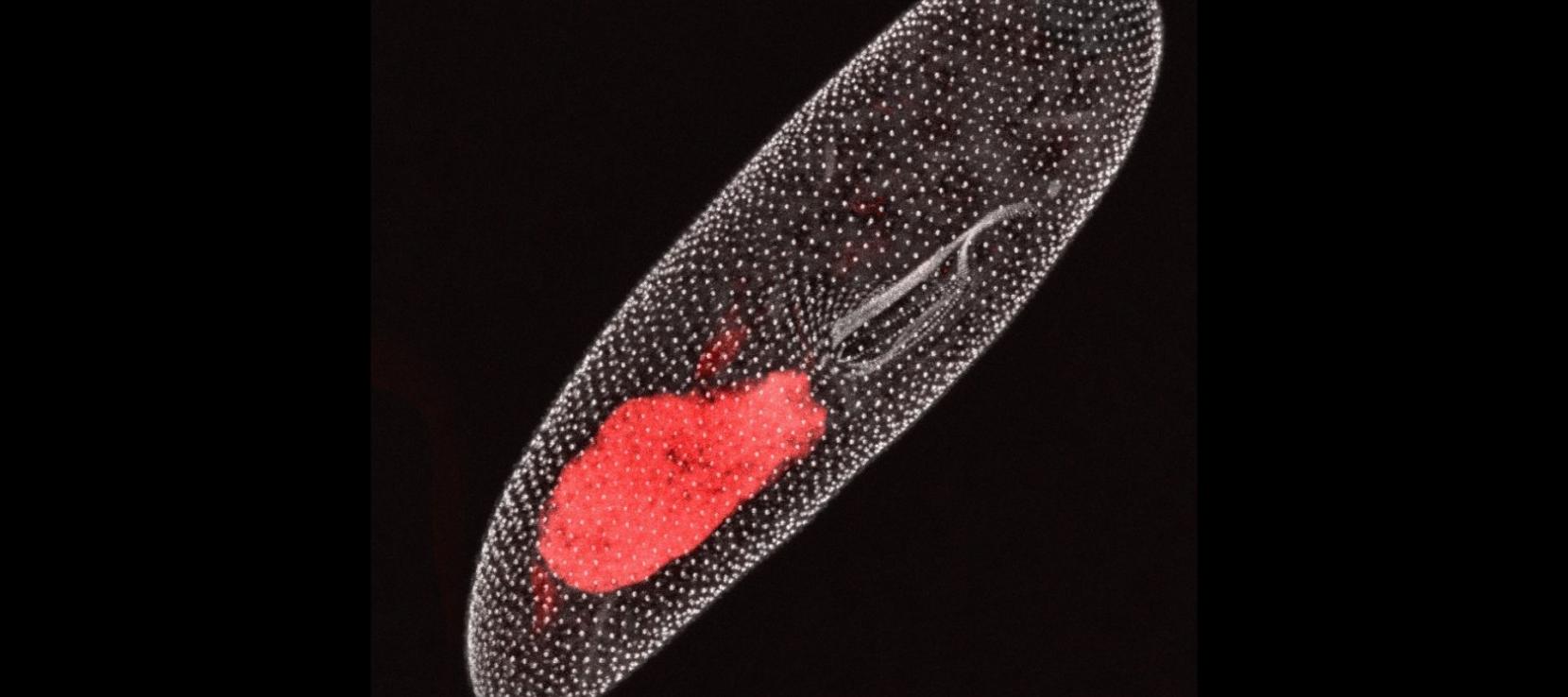
Mais il n’en va pas de même chez la paramécie, un unicellulaire au fonctionnement atypique, où les séquences répétées du génome sont éliminées à chaque cycle de reproduction sexuelle.
Dans les travaux publiés dans la revue Nature Communications, les chercheurs ont porté leur attention sur une protéine particulière : Ezl1. La caractéristique la plus surprenante de l’enzyme Ezl1, bien qu’elle présente des similarités de séquence et de structure avec la protéine humaine Ezh2, est qu’elle catalyse non pas une mais deux modifications chimiques : la sienne (H3K27) et celle d’une autre lysine (H3K9).
En combinant des tests enzymatiques in vitro et des expériences de génétique, ces travaux montrent donc que l’activité de cette enzyme a une plus large spécificité de substrats que précédemment décrite pour ce type de protéines. Des expériences de séquençage ont par ailleurs montré que les deux modifications de l’histone H3 sont déposées dans les mêmes régions du génome par cette enzyme au cours du développement, et conduisent au silence des éléments répétés, une fonction généralement dévolue à la seule modification K9.
Ces travaux suggèrent ainsi que ces deux modifications, souvent considérées comme ayant des fonctions distinctes, partagent en réalité une histoire évolutive commune et un rôle ancestral commun : celui de réduire au silence les éléments transposables.
« Deux modifications qui jouent des rôles redondants, c’est la première fois que l’on voit cela au niveau d’un génome entier, précise Sandra Duharcourt. C’est l’avantage de travailler sur des organismes différents comme la paramécie : regarder la diversité du vivant conduit à observer des choses que l’on n’avait pas anticipées. »
Pour en savoir plus > Lien vers la publication
Photo © : Andrea Frapporti, Caridad Miró Pina & Sandra Duharcourt